
尽管现代社会普遍面临食物过剩和肥胖问题,但人类在进化过程中形成的禁食生理机制依然存在。实际上,在全球某些地区,饥荒仍然是一个严峻的问题。禁食触发的代谢适应不仅帮助个体在食物短缺期间存活下来,还可能根据“节约基因假说”,在现代营养过剩的环境下促进肥胖的发生。此外,长期动物实验表明,热量限制和周期性禁食均有助于延长寿命,并带来其他健康益处。
然而,这些机制在人类中的具体作用、健康效益以及潜在风险尚未完全明确。为了更好地理解其临床应用潜力及安全性,迫切需要进一步研究以评估其可行性与风险控制措施。
近期,发表在Endocrine Reviews杂志上的一项综述,系统阐述了间歇禁食的生物学基础、适应性机制及其对代谢健康和寿命的潜在影响,尤其关注禁食对骨密度和骨骼健康的影响。此外,研究者审视了人类相关临床试验的现状,指出未来研究的必要方向和关键未解问题。

1.适应性禁食反应的三阶段模型
禁食开始后,人体经历三个经典适应阶段:早期利用肝脏和肌肉糖原分解供能;继而启动肝肾糖异生利用甘油和氨基酸生成葡萄糖;最终进入脂质代谢主导期,动员脂肪酸分解并启动肝脏酮体生成,供中枢神经系统能源需求。此转变为防止蛋白质过度消耗、延长禁食生存时间提供保障。
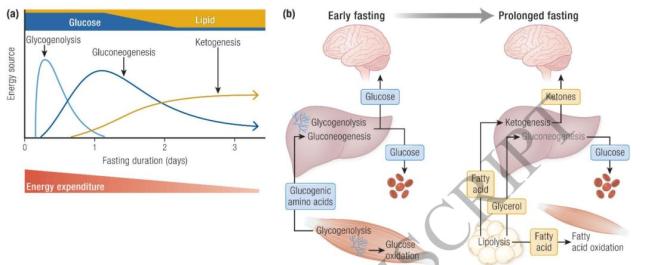
2.脂肪动员机制新进展
传统脂解途径包括脂肪三酯脂肪酶(ATGL)、激素敏感性脂肪酶(HSL)和单酰甘油脂肪酶(MGL)分步骤水解脂肪三酯,但近期发现非经典途径同样重要,例如溶酶体介导的脂解和脂滴以囊泡形式被巨噬细胞吞噬分解,丰富了脂肪动员的分子网络。
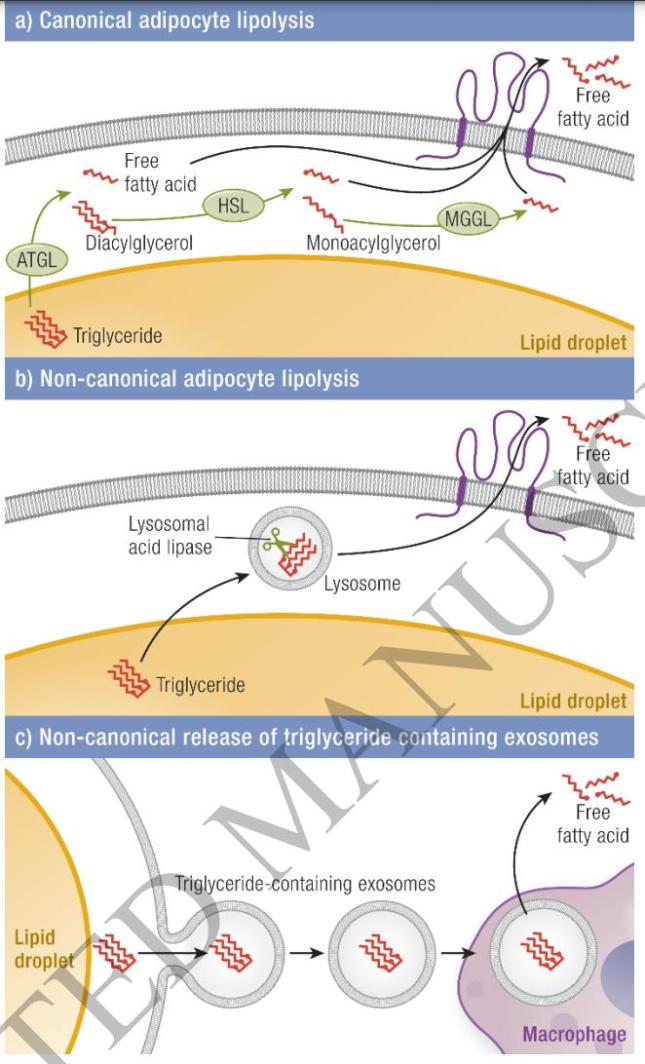
3.细胞能量底物转变
肌肉等组织在禁食时,胰岛素下降导致葡萄糖摄取减少,脂肪酸通过载体蛋白(CD36、FABPs)被优先摄取进入线粒体进行β-氧化,同时肝脏产生酮体确保脑部供能。
4.内分泌适应与代谢调控
禁食期间,瘦素水平显著下降,抑制下丘脑-垂体-甲状腺轴和生长激素-IGF-1轴,减少骨骼和生殖活动等非必需能量消耗。生长激素抵抗导致IGF-1下降,肝脏对GH信号响应减弱,避免能量用于生长。低瘦素是驱动这些适应性内分泌变化的关键因素,同时也关联促炎和免疫调节。
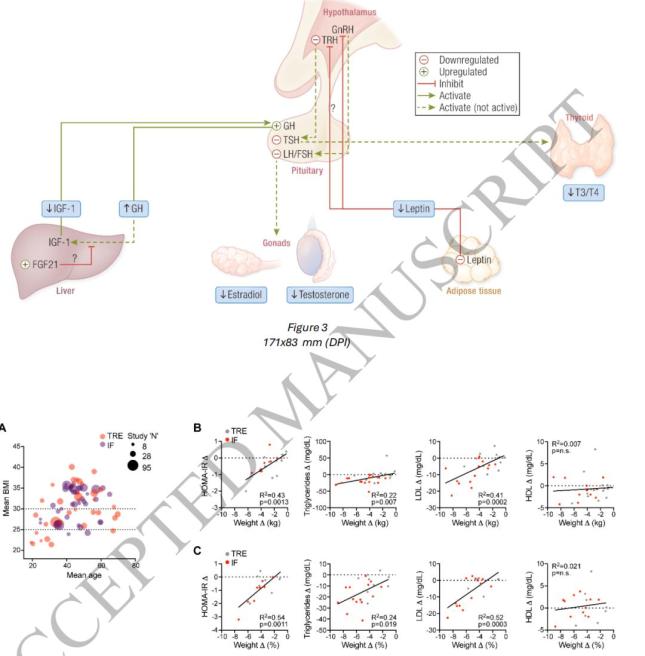
5.禁食的潜在益处与风险
益处包括促成体重下降,改善胰岛素敏感性,调节脂质组成,激活细胞自噬和蛋白酶体活性,可能通过代谢及表观遗传重编程延缓衰老,减少慢性炎症和相关癌症风险。
然而禁食亦伴随骨密度下降,骨折风险增加,尤其在慢性营养不良(如厌食症)患者中表现突出。禁食也可能引起某些类型的低度炎症和免疫功能损害。
6.人类临床研究现状
分析79项随机对照试验发现,多数研究对象为超重或肥胖成年人,禁食结合时限性进食多能显著减少体重,改善代谢指标(胰岛素抵抗、甘油三酯、LDL胆固醇),但禁食是否独立于减重产生代谢益处尚无定论。研究持续时间普遍较短,干预方式多样,缺乏长期大规模随机对照数据。
研究价值与意义
这篇综述系统整合了从机理到临床的间歇禁食相关证据,强调了禁食作为一种古老的生存策略,在现代代谢疾病和衰老预防领域的潜力及风险。其对机体内分泌、代谢的全面调控视角,深化了禁食影响的理解,尤其提出应关注禁食相关骨健康问题,提醒临床实践中需权衡利弊。此外,文章明确指出,目前的人体临床证据尚不足以完全支持禁食的广泛推广,呼吁未来设计更高质量、更长期的临床试验,并发展配套生物标志物以评估健康衰老。
原始出处
Fazeli PK, Steinhauser ML. A critical assessment of fasting to promote metabolic health and longevity. Endocr Rev. 2025. DOI:10.1210/endrev/bnaf021.
撰文 | 梅斯医学
编辑 | 阿拉斯加宝
● ●●版权说明:梅斯医学(MedSci)是国内领先的医学科研与学术服务平台,致力于医疗质量的改进,为临床实践提供智慧、精准的决策支持,让医生与患者受益。欢迎个人转发至朋友圈,谢绝媒体或机构未经授权以任何形式转载至其他平台。
原标题:《Endocrine Reviews:间歇性禁食如何影响代谢、衰老及骨骼健康?—— 机制与研究展望》